
Covid, 57 medici e scienziati chiedono lo stop immediato di tutte le vaccinazioni. Il documento
Esperti provenienti da tutto il mondo hanno espresso forti riserve sull’utilità delle campagne di massa per i profili di rischio rilevati. Il documento congiunto e le richieste avanzate alle Istituzioni
Un gruppo composto da 57 scienziati e medici provenienti da tutto il mondo ha reso noto un rapporto in cui viene messa in discussione la sicurezza e l’efficacia degli attuali vaccini COVID-19. Gli esperti con un documento preparatorio congiunto (che proponiamo – tradotto dall’inglese – di seguito) hanno chiesto la fine dei programmi di vaccinazione.
Vaccinazione di massa SARS-CoV-2: domande urgenti sulla sicurezza dei vaccini per ottenere risposte dalle agenzie sanitarie internazionali, dalle autorità di regolamentazione, dai governi e dagli sviluppatori di vaccini
Roxana Bruno 1 , Peter McCullough 2 , Teresa Forcades e Vila 3 , Alexandra Henrion-Caude 4 , Teresa García-Gasca 5 , Galina P. Zaitzeva 6 , Sally Priester 7 , María J. Martínez Albarracín 8 , Alejandro Sousa-Escandon 9 , Fernando López Mirones 10 , Bartomeu Payeras Cifre 11 , Almudena Zaragoza Velilla 10 , Leopoldo M. Borini 1 , Mario Mas 1 , Ramiro Salazar 1 , Edgardo Schinder 1 , Eduardo A Yahbes 1 , Marcela Witt 1, Mariana Salmeron 1 , Patricia Fernández 1 , Miriam M. Marchesini 1 , Alberto J. Kajihara 1 , Marisol V. de la Riva 1 , Patricia J. Chimeno 1 , Paola A. Grellet 1 , Matelda Lisdero 1 , Pamela Mas 1 , Abelardo J. Gatica Baudo 12 , Elisabeth Retamoza 12 , Oscar Botta 13 , Chinda C. Brandolino 13 , Javier Sciuto 14 , Mario Cabrera Avivar 14 , Mauricio Castillo 15 , Patricio Villarroel 15 , Emilia P. Poblete Rojas 15, Bárbara Aguayo 15 , Dan I. Macías Flores 15 , Jose V. Rossell 16 , Julio C. Sarmiento 17 , Victor Andrade-Sotomayor 17 , Wilfredo R. Stokes Baltazar 18 , Virna Cedeño Escobar 19 , Ulises Arrúa 20 , Atilio Farina del Río 21 , Tatiana Campos Esquivel 22 , Patricia Callisperis 23 , María Eugenia Barrientos 24 , Karina Acevedo-Whitehouse 5 , *
1 Epidemiologi metadisciplinari argentini. Repubblica argentina.
2 Baylor University Medical Center. Dallas, Texas, Stati Uniti.
3 Monestir de Sant Benet de Montserrat, Montserrat, Spagna
4 INSERM U781 Hôpital Necker-Enfants Malades, Université Paris Descartes-Sorbonne Cité, Institut Imagine, Parigi, Francia.
5 Scuola di Scienze Naturali. Università Autonoma di Querétaro, Querétaro, Messico.
6 Professore in pensione di Immunologia medica. Università di Guadalajara, Jalisco, Messico.
7 Medici per la verità Porto Rico. Ashford Medical Center. San Juan Portorico.
8 Professore in pensione di Processi diagnostici clinici. Università di Murcia, Murcia, Spagna
9Urologo Ospedale Comarcal de Monforte, Università di Santiago de Compostela, Spagna.
10 Biólogos por la Verdad, Spagna.
11 Biologo in pensione. Università di Barcellona. Specializzato in Microbiologia. Barcelona, Spagna.
12 Centro di Medicina Integrativa MICAEL (Centro Antroposófico Educando en Libertad di Medicina Integrativa). Mendoza, Repubblica Argentina.
13 Medici per la verità argentina. Repubblica argentina. ´
14 Medici per la verità Uruguay. Repubblica Orientale dell’Uruguay.
15 Medici per la libertà Cile. La Repubblica del Cile.
16 Medico, specialista ortopedico. La Repubblica del Cile.
17 Medici per la verità Perù. Repubblica del Perù.
18Medici per la verità Guatemala. Repubblica del Guatemala.
19 Concetto Azul SA Ecuador.
20 Medici per la verità Brasile. Brasile.
21 Medici per la verità Paraguay.
22 Medici per la Costa Rica.
23 Medici per la verità Bolivia.
24 Medici per la verità El Salvador.
* Corrispondenza: Karina Acevedo-Whitehouse, karina.acevedo.whitehouse@uaq.mx
Abstract
Dall’inizio dell’epidemia di COVID-19, la corsa per testare nuove piattaforme progettate per conferire immunità contro SARS-CoV-2 è stata dilagante e senza precedenti, portando all’autorizzazione di emergenza di vari vaccini. Nonostante i progressi nella terapia multipla precoce per i pazienti COVID-19, l’attuale mandato è quello di immunizzare la popolazione mondiale il più rapidamente possibile. La mancanza di test approfonditi sugli animali prima delle sperimentazioni cliniche e l’autorizzazione basata sui dati di sicurezza generati durante le prove che sono durate meno di tre mesi e mezzo, sollevano interrogativi riguardo alla sicurezza di questi vaccini. Il ruolo recentemente identificato del picco della glicoproteina SARS-CoV-2 nell’indurre il danno endoteliale caratteristico di COVID-19, anche in assenza di infezione, è estremamente rilevante dato che la maggior parte dei vaccini autorizzati induce la produzione di glicoproteina Spike nei riceventi. Dato l’elevato tasso di insorgenza di effetti avversi e l’ampia gamma di tipi di effetti avversi che sono stati segnalati fino ad oggi, nonché il potenziale di miglioramento della malattia guidato dal vaccino, immunopatologia Th2, autoimmunità ed evasione immunitaria, non c’è la necessità di una migliore comprensione dei benefici e dei rischi della vaccinazione di massa, in particolare nei gruppi che sono stati esclusi dalle sperimentazioni cliniche. Nonostante le richieste di cautela, i rischi della vaccinazione contro la SARS-CoV-2 sono stati ridotti al minimo o ignorati dalle organizzazioni sanitarie e dalle autorità governative. Facciamo appello alla necessità di un dialogo pluralistico nel contesto delle politiche sanitarie.
Introduzione
Da quando COVID-19 è stata dichiarata pandemia nel marzo 2020, sono stati segnalati oltre 150 milioni di casi e 3 milioni di decessi in tutto il mondo. Nonostante i progressi compiuti nella terapia ambulatoriale precoce e multifarmaco per pazienti ad alto rischio, con una riduzione dell’85% del ricovero e della morte per COVID-19 [1], l’attuale paradigma di controllo è la vaccinazione di massa. Pur riconoscendo lo sforzo richiesto per lo sviluppo, la produzione e l’autorizzazione di emergenza dei vaccini SARS-CoV-2, siamo preoccupati che i rischi siano stati ridotti al minimo o ignorati dalle organizzazioni sanitarie e dalle autorità governative, nonostante le richieste di cautela [2-8].
I vaccini per altri coronavirus non sono mai stati approvati per l’uomo e i dati generati nello sviluppo di vaccini contro il coronavirus progettati per suscitare anticorpi neutralizzanti mostrano che possono peggiorare la malattia COVID-19 tramite il potenziamento dipendente da anticorpi (ADE) e l’immunopatologia Th2, indipendentemente dal vaccino piattaforma e metodo di consegna [9-11]. È noto che il potenziamento della malattia guidato dai vaccini negli animali vaccinati contro SARS-CoV e MERS-CoV si verifica in seguito alla provocazione virale ed è stato attribuito agli immunocomplessi e alla cattura virale mediata da Fc da parte dei macrofagi, che aumentano l’attivazione e l’infiammazione delle cellule T [11 -13].
Nel marzo 2020, gli immunologi dei vaccini e gli esperti di coronavirus hanno valutato i rischi del vaccino SARS-CoV-2 sulla base di sperimentazioni sul vaccino SARS-CoV su modelli animali. Il gruppo di esperti ha concluso che l’ADE e l’immunopatologia costituivano una vera preoccupazione, ma ha affermato che il loro rischio era insufficiente per ritardare gli studi clinici, sebbene sarebbe necessario un monitoraggio continuo [14]. Sebbene non vi sia una chiara evidenza del verificarsi di ADE e immunopatologia correlata al vaccino in volontari immunizzati con vaccini SARS-CoV-2 [15], gli studi di sicurezza fino ad oggi non hanno affrontato specificamente questi gravi effetti avversi (SAE). Dato che il follow-up dei volontari non ha superato i 2-3,5 mesi dopo la seconda dose [16-19], è improbabile che tale SAE sia stato osservato. Nonostante 92 errori nella segnalazione, non si può ignorare che anche tenendo conto del numero di vaccini somministrati, secondo il Vaccine Adverse Effect Reporting System (VAERS) degli Stati Uniti, il numero di decessi per milione di dosi di vaccino somministrate è aumentato di oltre 10 volte. Riteniamo che sia urgentemente necessario un dialogo scientifico aperto sulla sicurezza dei vaccini nel contesto dell’immunizzazione su larga scala. In questo documento, descriviamo alcuni dei rischi della vaccinazione di massa nel contesto dei criteri di esclusione della sperimentazione di fase 3 e discutiamo il SAE riportato nei sistemi di registrazione degli effetti avversi nazionali e regionali. Evidenziamo le domande senza risposta e attiriamo l’attenzione sulla necessità di un approccio più cauto alla vaccinazione di massa.
Criteri di esclusione dallo studio SARS-CoV-2 di fase 3
Con poche eccezioni, gli studi sul vaccino SARS-CoV-2 hanno escluso gli anziani [16-19], rendendo impossibile identificare l’insorgenza di eosinofilia post-vaccinazione e maggiore infiammazione negli anziani. Studi sui vaccini SARS-CoV hanno mostrato che i topi anziani immunizzati erano particolarmente a rischio di immunopatologia Th2 pericolosa per la vita [9,20]. Nonostante queste prove e i dati estremamente limitati sulla sicurezza e l’efficacia dei vaccini SARS-CoV-2 negli anziani, le campagne di vaccinazione di massa si sono concentrate fin dall’inizio su questa fascia di età. La maggior parte degli studi ha escluso anche volontarie in gravidanza e in allattamento, nonché quelle con condizioni croniche e gravi come la tubercolosi, l’epatite C, l’autoimmunità, le coagulopatie, il cancro e la soppressione immunitaria [16-29], sebbene a questi riceventi venga ora offerto il vaccino sotto la premessa della sicurezza.
Un altro criterio di esclusione da quasi tutti gli studi era l’esposizione precedente a SARS-CoV-2. Questo è un peccato in quanto ha negato l’opportunità di ottenere informazioni estremamente rilevanti sull’ADE post-vaccinazione in persone che hanno già anticorpi anti-SARS-Cov-2. Per quanto a nostra conoscenza, l’ADE non viene monitorato sistematicamente per nessun gruppo di età o condizione medica a cui viene attualmente somministrato il vaccino. Inoltre, nonostante una proporzione sostanziale della popolazione abbia già anticorpi [21], i test per determinare lo stato degli anticorpi SARS-CoV-2 prima della somministrazione del vaccino non vengono condotti di routine.
Gli effetti avversi gravi dei vaccini SARS-CoV-2 passeranno inosservati?
COVID-19 comprende un ampio spettro clinico, che va da patologie polmonari molto lievi a gravi e malattie multiorgano fatali con disregolazione infiammatoria, cardiovascolare e della coagulazione del sangue [22-24]. In questo senso, i casi di ADE o immunopatologia correlati al vaccino sarebbero clinicamente indistinguibili dal COVID-19 grave [25]. Inoltre, anche in assenza del virus SARS-CoV-2, la sola glicoproteina Spike provoca danni endoteliali e ipertensione in vitro e in vivo nei criceti siriani, riducendo l’enzima di conversione dell’angiotensina 2 (ACE2) e compromettendo la funzione mitocondriale [26]. Sebbene questi risultati debbano essere confermati negli esseri umani, le implicazioni di questo risultato sono sconcertanti, poiché tutti i vaccini autorizzati per l’uso di emergenza si basano sulla somministrazione o sull’induzione della sintesi di glicoproteine Spike. Nel caso dei vaccini con mRNA e dei vaccini vettorizzati con adenovirus, nessuno studio ha esaminato la durata della produzione di Spike negli esseri umani dopo la vaccinazione. In base al principio di cautela, è parsimonioso considerare che la sintesi di Spike indotta dal vaccino potrebbe causare segni clinici di COVID-19 grave ed essere erroneamente conteggiata come nuovi casi di infezioni da SARS-CoV-2. In tal caso, i veri effetti negativi dell’attuale strategia di vaccinazione globale potrebbero non essere mai riconosciuti a meno che gli studi non esaminino specificamente questa domanda. Esistono già prove non causali di aumenti temporanei o prolungati in 138 dei decessi per COVID-19 a seguito della vaccinazione in alcuni paesi (Fig.1). Alla luce della patogenicità di Spike, questi decessi devono essere studiati in profondità per determinare se sono correlati alla vaccinazione. ma non un singolo studio ha esaminato la durata della produzione di Spike negli esseri umani dopo la vaccinazione.
Reazioni avverse impreviste ai vaccini SARS-CoV-2
Un altro problema critico da considerare data la scala globale della vaccinazione contro la SARS-CoV-2 è l’autoimmunità. SARS-CoV-2 ha numerose proteine immunogeniche e tutti i suoi epitopi immunogenici tranne uno hanno somiglianze con le proteine umane [27]. Questi possono agire come una fonte di antigeni, portando all’autoimmunità [28]. Mentre è vero che gli stessi effetti potrebbero essere osservati durante l’infezione naturale da SARS-CoV-2, la vaccinazione è destinata alla maggior parte della popolazione mondiale, mentre si stima che solo il 10% della popolazione mondiale sia stata infettata da SARS-CoV -2, secondo il dottor Michael Ryan, responsabile delle emergenze presso l’Organizzazione mondiale della sanità. Non siamo stati in grado di trovare prove che uno qualsiasi dei vaccini attualmente autorizzati abbia selezionato ed escluso epitopi immunogenici omologhi per evitare la potenziale autoimmunità dovuta all’innesco patogeno.
Alcune reazioni avverse, compresi i disturbi della coagulazione del sangue, sono già state segnalate in soggetti sani e giovani vaccinati. Questi casi hanno portato alla sospensione o all’annullamento dell’uso dei vaccini ChAdOx1-nCov-19 e Janssen adenovirali vettorizzati in alcuni paesi. È stato ora proposto che la vaccinazione con ChAdOx1-nCov-19 possa provocare trombocitopenia trombotica immunitaria (VITT) mediata da anticorpi attivanti le piastrine contro il fattore piastrinico-4, che clinicamente imita la trombocitopenia autoimmune indotta da eparina [29]. Sfortunatamente, il rischio è stato trascurato quando si autorizzano questi vaccini, sebbene la trombocitopenia indotta da adenovirus sia nota da più di un decennio e sia stato un evento coerente con i vettori adenovirali [30]. Il rischio di VITT sarebbe presumibilmente più alto in quelli già a rischio di coaguli di sangue.
A livello di popolazione, potrebbero esserci anche impatti legati ai vaccini. SARS-CoV-2 è un virus a RNA a rapida evoluzione che finora ha prodotto più di 40.000 varianti [32,33] alcune delle quali influenzano il dominio antigenico della glicoproteina Spike [34,35]. Dati gli alti tassi di mutazione, la sintesi indotta dal vaccino di alti livelli di anticorpi anti-SARS-CoV-2-Spike potrebbe teoricamente portare a risposte non ottimali contro infezioni successive da altre varianti in individui vaccinati [36], un fenomeno noto come “antigenico originale sin ”[37] o priming antigenico [38]. Non è noto fino a che punto le mutazioni che influenzano l’antigenicità della SARS-CoV-2 si fisseranno durante l’evoluzione virale [39], ma i vaccini potrebbero plausibilmente agire come forze selettive che guidano varianti con maggiore infettività o trasmissibilità. Considerando l’elevata somiglianza tra le varianti note di SARS-CoV-2, questo scenario è improbabile [32,34] ma se le varianti future dovessero differire maggiormente negli epitopi chiave, la strategia di vaccinazione globale potrebbe aver contribuito a formare un virus ancora più pericoloso. Questo rischio è stato recentemente portato all’attenzione dell’OMS come lettera aperta [40].
Discussione
I rischi qui delineati sono un grosso ostacolo alla prosecuzione della vaccinazione globale contro la SARS-CoV-2. La prova sulla sicurezza di tutti i vaccini SARS-CoV-2 è necessaria prima di esporre più persone al rischio di questi esperimenti, poiché il rilascio di un vaccino candidato senza tempo per comprendere appieno l’impatto risultante sulla salute potrebbe portare a un’esacerbazione dell’attuale crisi globale. [41]. La stratificazione del rischio dei soggetti vaccinati è essenziale. Secondo il governo del Regno Unito, le persone di età inferiore ai 60 anni hanno un rischio estremamente basso di morire per COVID-191187. Tuttavia, secondo Eudravigillance, la maggior parte degli effetti avversi gravi a seguito della vaccinazione SARS-CoV-2 si verificano in persone di età compresa tra 18 e 64 anni. Di particolare interesse è il programma di vaccinazione previsto per i bambini dai 6 anni in su negli Stati Uniti e nel Regno Unito. Dott. Anthony Fauci ha recentemente anticipato che gli adolescenti di tutto il paese saranno vaccinati in autunno e i bambini più piccoli all’inizio del 2022, e il Regno Unito è in attesa dei risultati dei test per iniziare la vaccinazione di 11 milioni di bambini sotto i 18 anni. Mancano giustificazioni scientifiche per sottoporre bambini sani ai vaccini sperimentali, dato che il Centers for Disease Control and Prevention stima che abbiano un tasso di sopravvivenza del 99,997% se infettati da SARS-CoV-2. Non solo il COVID-19 è irrilevante come minaccia per questo gruppo di età, ma non ci sono prove affidabili a sostegno dell’efficacia o dell’efficacia del vaccino in questa popolazione o per escludere effetti collaterali dannosi di questi vaccini sperimentali. In questo senso, quando i medici consigliano ai pazienti la somministrazione elettiva della vaccinazione COVID-19.
In conclusione, nel contesto della frettolosa autorizzazione all’uso di emergenza dei vaccini SARS-CoV-2 e delle attuali lacune nella nostra comprensione della loro sicurezza, devono essere sollevate le seguenti domande:
- È noto se gli anticorpi cross-reattivi di precedenti infezioni da coronavirus o il vaccino e gli anticorpi indotti possono influenzare il rischio di patogenesi non intenzionale dopo la vaccinazione con COVID-19?
- Il rischio specifico di ADE, immunopatologia, autoimmunità e reazioni avverse gravi è stato chiaramente rivelato ai destinatari del vaccino per soddisfare lo standard di etica medica di comprensione del paziente per il consenso informato? In caso negativo, quali sono i motivi e come potrebbe essere implementato?
- Qual è la logica alla base della somministrazione del vaccino a ogni individuo quando il rischio di morte per COVID-19 non è uguale tra i gruppi di età e le condizioni cliniche e quando gli studi di fase 3 hanno escluso anziani, bambini e condizioni specifiche frequenti?
- Quali sono i diritti legali dei pazienti se vengono danneggiati da un vaccino SARS-CoV-2? Chi coprirà i costi delle cure mediche? Se i reclami dovessero essere risolti con denaro pubblico, il pubblico è stato informato che ai produttori di vaccini è stata concessa l’immunità e la loro responsabilità di risarcire coloro che sono stati danneggiati dal vaccino è stata trasferita ai contribuenti?
Nel contesto di queste preoccupazioni, proponiamo di interrompere la vaccinazione di massa e di aprire un dialogo urgente pluralistico, critico e scientificamente fondato sulla vaccinazione SARS-CoV-2 tra scienziati, medici, agenzie sanitarie internazionali, autorità di regolamentazione, governi e vaccini sviluppatori. Questo è l’unico modo per colmare l’attuale divario tra le prove scientifiche e la politica di salute pubblica per quanto riguarda i vaccini SARS-CoV-2. Siamo convinti che l’umanità meriti una comprensione più profonda dei rischi rispetto a quella che attualmente viene propagandata come posizione ufficiale. Un dialogo scientifico aperto è urgente e indispensabile per evitare l’erosione della fiducia del pubblico nella scienza e nella salute pubblica e per garantire che l’OMS e le autorità sanitarie nazionali proteggano gli interessi dell’umanità durante l’attuale pandemia. È urgente riportare la politica di sanità pubblica alla medicina basata sull’evidenza, basandosi su un’attenta valutazione della ricerca scientifica pertinente. È imperativo seguire la scienza.
Dichiarazione di conflitto di interessi
Gli autori dichiarano che la ricerca è stata condotta in assenza di rapporti commerciali o finanziari che potrebbero essere interpretati come un potenziale conflitto di interessi.
Riferimenti
- McCullough PA, Alexander PE, Armstrong R, et al. Trattamento multifarmaco sequenziale altamente mirato multiforme dell’infezione precoce ambulatoriale ad alto rischio di SARS-CoV-2 (COVID-19). Rev Cardiovasc Med (2020) 21: 517–530. doi: 10.31083 / j.rcm.2020.04.264
- Arvin AM, Fink K, Schmid MA, et al. Una prospettiva sul potenziamento potenziale anticorpo-dipendente di SARS-CoV-2. Nature (2020) 484: 353–363. doi: 10.1038 / s41586-020-2538-8
- Coish JM, MacNeil AJ. Fuori dalla padella e nel fuoco? Due diligence garantite per ADE in COVID-19. Microbes Infect (2020) 22 (9): 405-406. doi: 10.1016 / j.micinf.2020.06.006
- Eroshenko N, Gill T, Keaveney ML, et al. Implicazioni del potenziamento dell’infezione anticorpo-dipendente per le contromisure SARS-CoV-2. Nature Biotechnol (2020) 38: 788–797. doi: 10.1038 / s41587-020-0577-1
- Polonia GA. Tartarughe, lepri e vaccini: una nota cautelativa per lo sviluppo del vaccino SARS-CoV-2. Vaccine (2020) 38: 4219–4220. doi: 10.1016 / j.vaccine.2020.04.073
- Shibo J. Non affrettarti a distribuire vaccini e farmaci COVID-19 senza sufficienti garanzie di sicurezza. Nature (2000) 579,321. doi: 10.1038 / d41586-020-00751-9
- Munoz FA, Cramer JP, Dekker CL, et al. Malattia potenziata associata a vaccino: definizione del caso e linee guida per la raccolta dei dati, l’analisi e la presentazione dei dati sulla sicurezza dell’immunizzazione. Vaccine (2021) https://doi.org/10.1016/j.vaccine.2021.01.055
- Cardozo T, Veazey R. Divulgazione del consenso informato ai soggetti di sperimentazione sui vaccini di rischio di vaccini COVID-19 che peggiorano la malattia clinica. Int J Clin Pract (2020) 28: e13795. doi: 10.1111 / ijcp.13795
- Bolles D, Long K, Adnihothram S, et al. Un vaccino contro il coronavirus per la sindrome respiratoria acuta grave a doppia inattivazione fornisce una protezione incompleta nei topi e induce una maggiore risposta polmonare proinfiammatoria eosinofila alla provocazione. J Virol (2001) 85: 12201–12215. doi: 10.1128 / JVI.06048-11
- Weingartl H, Czub M, Czub S, et al. L’immunizzazione con il vaccino ricombinante a base di virus ancarabico modificato contro la sindrome respiratoria acuta grave è associata a un’epatite potenziata nei furetti. J Virol (2004) 78: 12672–12676. doi: 10.1128 / JVI.78.22.12672-12676.2004272
- Tseng CT, Sbrana E, Iwata-Yoshikawa N, et al. L’immunizzazione con i vaccini contro il coronavirus della SARS porta all’immunopatologia polmonare contro il virus della SARS. PLoS One (2012) 7 (4): e35421. doi: 10.1371 / journal.pone.0035421
- Iwasaki A, Yang Y. Il potenziale pericolo di risposte anticorpali non ottimali in COVID-19. Nat Rev Immunol (2020) 20: 339–341. doi: 10.1038 / s41577-020-0321-6
- Vennema H, de Groot RJ, Harbor DA, et al. Morte prematura dopo la stimolazione del virus della peritonite infettiva felina a causa dell’immunizzazione del virus vaccinico ricombinante. J Virol (1990) 64: 1407-1409
- Lambert PH, Ambrosino DM, Andersen SR, et al. Consensus summary report for CEPI / BC March 12-13, 2020 meeting: Assessment of risk of disease enhancement with COVID-19 vaccines. Vaccino (2020) 38 (31): 4783-4791. doi: 10.1016 / j.vaccine.2020.05.064
- de Alwis R, Chen S, Gan S, et al. Impatto del potenziamento immunitario sulla terapia con globuline iperimmuni policlonali Covid-19 e sullo sviluppo di vaccini. EbioMedicine (2020) 55: 102768. doi: 10.1016 / j.ebiom.2020.102768
- Folegatti PM, Ewer KJ, Aley PK, et al. Sicurezza e immunogenicità del vaccino ChAdOx1 nCoV? 287 19 contro SARS-CoV-2: un rapporto preliminare di uno studio di fase 1/2, in singolo cieco, randomizzato controllato. Lancet (2020) 396: 467–783. doi: 10.1016 / S0140-6736 (20) 31604-4
- Polack FP, Thomas SJ, Kitchin N. Sicurezza ed efficacia del vaccino BNT162b2 mRNA Covid-19. N Engl J Med (2020) 383: 2603–2615. doi: 10.1056 / NEJMoa2034577
- Ramasamy MN, Minassian AM, Ewer KJ, et al. Sicurezza e immunogenicità del vaccino ChAdOx1 nCoV-19 somministrato in regime di prime-boost in adulti giovani e anziani (COV002): uno studio di fase 2/3 in singolo cieco, randomizzato, controllato. Lancet (2021) 396: 1979–93. doi: 10.1016 / S0140-6736 (20) 32466-1
- Chu L, McPhee R, Huang W, et al. Gruppo di studio mRNA-1273. Un rapporto preliminare di uno studio di fase 2 controllato randomizzato sulla sicurezza e l’immunogenicità del vaccino mRNA-1273 SARS-CoV-2. Vaccino (2021) S0264-410X (21) 00153-5. doi: 10.1016 / j.vaccine.2021.02.007
- Liu L, Wei Q, Lin Q, et al. Le IgG anti-spike provocano gravi lesioni polmonari acute alterando le risposte dei macrofagi durante l’infezione acuta da SARS-CoV. JCI Insight (2019) 4 (4): e123158. doi: 10.1172 / jci.insight.123158.
- Ioannidis PA. Tasso di mortalità per infezione del COVID-19 desunto dai dati di sieroprevalenza. Bull WHO (2021) 99: 19–33 F. http://dx.doi.org/10.2471/BLT.20.265892
- Martines RB, Ritter JM, Matkovic E, et al. Patologia e patogenesi della SARS-CoV-2 associata a malattia da coronavirus fatale, Stati Uniti Emerg Infect Dis (2020) 26: 2005-2015. doi: 10.3201 / eid2609.202095
- Wu Z, McGoogan JM. Caratteristiche e lezioni importanti dell’epidemia di coronavirus 2019 (COVID-19) in Cina: riepilogo di un rapporto di 72.314 casi del Centro cinese per il controllo e la prevenzione delle malattie. JAMA (2020) 323: 1239-1242. doi: 10.1001 / jama.2020.2648
- Xu Z, Shi L, Wang Y, et al. Reperti patologici di COVID-19 associati a sindrome da distress respiratorio acuto. Lancet Respiratory Med (2020) 8: 420-422 doi: 10.1016 / S2213-2600 (20) 30076-X
- Negro F. Il potenziamento dipendente dagli anticorpi gioca un ruolo nella patogenesi di COVID-19? Swiss Medical Weekly (2020) 150: w20249. doi: 10.4414 / smw.2020.20249317
- Lei Y, Zhang J, Schiavon CR et al., Spike Protein altera la funzione endoteliale tramite la downregulation di ACE 2. Circulation Res (2021) 128: 1323-1326. https://doi.org/10.1161/CIRCRESAHA.121.318902
- Lyons-Weiler J. L’innesco patogeno probabilmente contribuisce a malattie e mortalità gravi e critiche in COVID-19 tramite autoimmunità, J Translational Autoimmunity (2020) 3: 100051. doi: 10.1016 / j.jtauto.2020.100051
- An H, Park J. Molecular Mimicry Map (3M) di SARS-CoV-2: previsione di epitopi SARS-CoV-2 potenzialmente immunopatogeni tramite un nuovo approccio immunoinformatico. bioRxiv [Preprint]. 12 novembre 2020 [citato il 19 aprile 2020] https://doi.org/10.1101/2020.11.12.344424
- Greinacher A, Thiele T, Warkentin TE, Weisser K, Kyrle PA, Eichinger S. Thrombotic Thrombocytopenia dopo vaccinazione con ChAdOx1 nCov-19. N Engl J Med (2021). doi: 10.1056 / NEJMoa2104840
- Othman M, Labelle A, Mazzetti I et al. Trombocitopenia indotta da adenovirus: il ruolo del fattore di von Willebrand e della P-selectina nel mediare la clearance piastrinica accelerata. Blood (2007) 109: 2832–2839. doi: 10.1182 / blood-2006-06-032524
- Ortel TL. Fattori di rischio trombotici acquisiti in ambito di terapia intensiva. Crit Care Med (2010) 38 (2 Suppl): S43-50. doi: 10.1097 / CCM.0b013e3181c9ccc8
- Grubaugh ND, Petrone ME, Holmes EC. Non dovremmo preoccuparci quando un virus muta durante i focolai della malattia. Nat Microbiol (2020) 5: 529-530. https://doi.org/10.1038/s41564-020-0690-4
- Greaney AJ, Starr TN, Gilchuk P, et al. Mappatura completa delle mutazioni nel dominio di legame al recettore SARS-CoV339 2 Spike che sfugge al riconoscimento degli anticorpi. Cell Host Microbe (2021) 29: 44–57.e9. doi: 10.1016 / j.chom.2020.11.007.
- Lauring AS, Hodcroft EB. Varianti genetiche di SARS-CoV-2: cosa significano? JAMA (2021) 325: 529–531. doi: 10.1001 / jama.2020.27124
- Zhang L, Jackson CB, Mou H, et al. La mutazione D614G nella proteina spike SARS-CoV-2 riduce la diffusione di S1 e aumenta l’infettività. bioRxiv [Preprint]. 12 giugno 2020 [citato 2021 aprile 19] https://doi.org/10.1101/2020.06.12.148726
- Korber B, Fischer WM, Gnanakaran S et al. Sheffield COVID-19 Genomics Group. Rilevamento dei cambiamenti nel picco di SARS-CoV-2: prova che D614G aumenta l’infettività del virus COVID-19. Cella (2020) 182: 812-827.e19. doi: 10.1016 / j.cell.2020.06.043
- Francis T. Sulla dottrina del peccato antigenico originale. Proc Am Philos Soc (1960) 104: 572–578.
- Vibroud C, Epstein SL. La prima influenza è per sempre. Science (2016) 354: 706–707. doi: 10.1126 / science.aak9816
- Weisblum Y, Schmidt F, Zhang F, et al. Fuga dagli anticorpi neutralizzanti dalle varianti della proteina spike di SARS? 354 CoV-2. Elife (2020) 9: e61312. doi: 10.7554 / eLife.61312
- Vanden Bossche G (6 marzo 2021) https://dryburgh.com/wp-356content/uploads/2021/03/Geert_Vanden_Bossche_Open_Letter_WHO_March_6_2021.pdf
- Coish JM, MacNeil AJ. Fuori dalla padella e nel fuoco? Due diligence garantite per ADE in COVID-19. Microbes Infect (2020) 22 (9): 405-406. doi: 10.1016 / j.micinf.2020.06.006
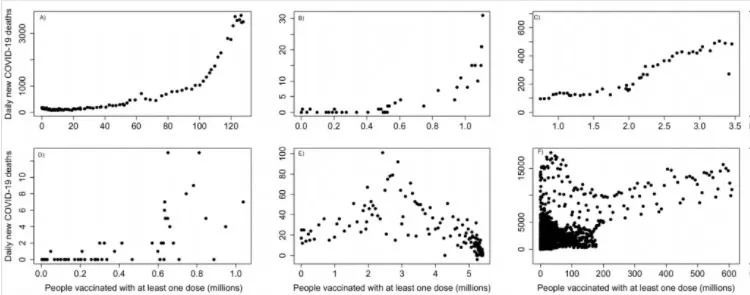
Legenda delle figure
Figura 1. Numero di nuovi decessi per COVID-19 in relazione al numero di persone che hanno ricevuto almeno una dose di vaccino per paesi selezionati. Il grafico mostra i dati dall’inizio della vaccinazione al 3 maggio 365, 2021. A) India (9,25% della popolazione vaccinata), B) Thailandia (1,58% della popolazione vaccinata), C) Colombia (6,79% della popolazione vaccinata), D) Mongolia (31,65% della popolazione vaccinata), E) Israele (62,47% della popolazione vaccinata), F) Mondo intero (7,81% della popolazione vaccinata). I grafici sono stati costruiti utilizzando i dati di Our World in Data (accesso 4 maggio 2021) https://github.com/owid/covid-19-data/tree/master/public/data/vaccinations
Rec News dir. Zaira Bartucca – recnews.it
COVID
Verso il reintegro dei sanitari non vaccinati
“Il Ministro della Salute Orazio Schillaci, a sei mesi dalla sospensione dello stato d’emergenza e in considerazione dell’andamento del contagio da Covid-19, ritiene opportuno avviare un progressivo ritorno alla normalità nelle attività e nei comportamenti, ispirati a criteri di responsabilità e rispetto delle norme vigenti”. E’ quanto si legge in un comunicato stampa del ministero della salute.
“Pertanto anche in base alle indicazioni prevalenti in ambito medico e scientifico, si procederà alla sospensione della pubblicazione giornaliera del bollettino dei dati relativi alla diffusione dell’epidemia, ai ricoveri e ai decessi, che sarà ora reso noto con cadenza settimanale, fatta salva la possibilità per le autorità competenti di acquisire in qualsiasi momento le informazioni necessarie al controllo della situazione e all’adozione dei provvedimenti del caso”.

Il ministro della Salute Orazio Schillaci
“Per quanto riguarda il personale sanitario soggetto a procedimenti di sospensione per inadempienza all’obbligo vaccinale e l’annullamento delle multe previste dal dl 44/21 – fa sapere ancora il ministero della Salute – in vista della scadenza al prossimo 31 dicembre delle disposizioni in vigore e della preoccupante carenza di personale medico e sanitario segnalata dai responsabili delle strutture sanitarie e territoriali è in via di definizione un provvedimento che consentirà il reintegro in servizio del suddetto personale prima del termine di scadenza della sospensione”.
COVID
Ed è subito farsa. Il governo pensa di dare la presidenza della Commissione d’inchiesta sul covid all’opposizione

Ciriani sulla Commissione d’inchiesta covid
La presidenza della Commissione d’inchiesta sul covid all’opposizione. Il governo Meloni ci sta pensando, e anzi sull’argomento si è espresso questa mattina il ministro per i Rapporti con il Parlamento Luca Ciriani. “E’ una cosa che possiamo prendere in considerazione. Questa commissione sarebbe dovuta nascere la scorsa legislatura Renzi l’aveva annunciata ma poi non se ne è fatto nulla con la campagna elettorale. Io penso che una commissione di indagine possa nascere, potrebbe anche essere che la guidi un esponente dell’opposizione, ma che la guidi un esponente dell’opposizione o maggioranza, io credo che vada fatta luce sulla gestione di fondi pubblici in maniera molto molto opaca, se c’è la commissione che indaga su questo per me è la benvenuta”.
Silenzio da parte del governo sulla campagna di vaccinazione di massa e sulle e misure liberticide
Ciriani, come già la Meloni nel corso del discorso per chiedere la Fiducia alla Camera, parla inoltre di “gestione dei fondi pubblici”. Eppure la conduzione della pandemia da parte dei governi Conte II e Draghi non è certo stata caratterizzata solo da questo, né tutto si è esaurito con la cresta sulle mascherine o con il ruolo del commissario Arcuri. Ci sono la campagna di vaccinazione di massa, i contratti con le multinazionali farmaceutiche, l’imposizione del Green Pass negli uffici pubblici (su cui FdI non ha interesse a indagare, essendo stato partito promotore del certificato verde), il lockdown quasi totale per un virus che oggi Bassetti ammette si poteva curare con l’aspirina, la caccia ai non mascherati, la discriminazione sistematica dei non vaccinati, la cancellazione del diritto al lavoro, l’utilizzo improprio delle auto-certificazioni, le chiusure evitabili delle attività commerciali. Non da ultimo, i danneggiati dai vaccini (anche in maniera permanente) e i deceduti. Su tutto questo dovrebbe fare luce una Commissione d’inchiesta parlamentare degna di questo nome, ma gli esordi – con l’idea di consegnarne la presidenza a un componente dell’opposizione o a qualche duttile renziano – non sembrano essere dei migliori.
COVID
Se ne accorgono solo ora: il covid si cura anche con dei banali anti-infiammatori
Chi, come noi, lo diceva due anni fa era un “complottista” che pubblica “fake news”. Adesso, con appena 24 mesi di ritardo, l’Istituto Mario Negri ha svelato l’arcano: il covid si cura e tanto possono fare – per approcciarsi al virus – dei banali anti-infiammatori

Chi, come noi, lo diceva due anni fa era un “complottista” che pubblica “fake news”. Adesso, con appena 24 mesi di ritardo, l’Istituto Mario Negri ha svelato l’arcano: il covid si cura e tanto possono fare – per approcciarsi al virus – dei banali anti-infiammatori. Rec News ha iniziato a parlare di cure già all’inizio del 2020, quando pubblicava i documenti di studi resi noti all’estero e intervistava medici autorevoli che purtroppo non sono stati ascoltati da chi ricopriva ruoli decisionali.
Oggi gli scienziati e i virostar come Remuzzi, che ha preso parte allo studio del Mario Negri, giungono a questa conclusione dopo decine di migliaia di persone morte senza essere state curate al manifestarsi dei sintomi, dopo che soggetti con altre malattie sono stati lasciati fuori dagli ospedali e dopo che altri sono stati abbandonati a loro stessi anche quando dovevano sottoporsi a operazioni chirurgiche.
Senza contare i vaccinati, danneggiati o morti per colpa di un siero sperimentale cui si sono affidati senza remore, nella convinzione che non esistesse alternativa: questo hanno fatto credere i governi Conte e Draghi, questo ha fatto passare la stampa mainstream.
Scrive ora Ansa:
La terapia a base di antinfiammatori (in particolare non steroidei, i Fans), avviata all’inizio dei sintomi, riduce il rischio di ospedalizzazione per Covid dell’85-90% Dopo due anni e mezzo di pandemia la comunità scientifica concorda su un punto: a uccidere i malati è l’infiammazione (o flogosi), non il virus.
Ricapitolando: due anni di privazioni, mascherine, isteria, ipocondria, allarmismi ingiustificati, corse all’hub vaccinale, bambini usati come cavie e anziani immolati per un virus che, se il sistema immunitario non fa il suo lavoro, si può curare con delle bustine di anti-infiammatorio?
Possibile che nessuno si sia accorto prima – a virus, come si sostiene, “isolato” – che principi attivi conosciuti, in genere ben tollerati e presenti in tutte le case avrebbero potuto fare in modo che si evitasse la campagna di vaccinazione di massa, cioè la sperimentazione umana di un siero di cui si saprà di più solo nel 2023? Nessuno, dunque, che risponda per la baracca emergenziale messa in piedi, che non ha avuto eguali in Europa e forse nel mondo e che – ci dicono oggi gli scienziati tra le righe – si poteva evitare?
“Covid, gli antinfiammatori riducono le ospedalizzazioni del 90%” in Corriere della Sera del 26/08/22
“Covid: con antinfiammatori riduzione del 90% dei ricoveri” – in Ansa del 26/08/22
Rec News dir. Zaira Bartucca – recnews.it
COVID
Covid, fioccano denunce e querele per Draghi e per Figliuolo
Il generale accusato di omicidio colposo, crimini contro l’Umanità, abuso di autorità, violenza privata, procurato allarme e diffusione di notizie false. Premier e governo denunciati a Messina, a Biella e nel Varesotto per sequestro di persona e per la discriminazione dei non vaccinati. La querela di ALI – Avvocati Liberi per i “delitti commessi contro la personalità dello Stato”

Fioccano denunce e querele per il presidente del Consiglio Mario Draghi e per il commissario all’Emergenza sanitaria Francesco Paolo Figliuolo. Provengono da tutta Italia e sembra si moltiplichino a ogni passo (falso), a ogni acuirsi delle restrizioni e a ogni protrarsi di provvedimenti anticostituzionali. Una bella gatta da pelare per i due, tanto che all’ex “generalissimo” prontamente è stato tolto il comando della Logistica dell’Esercito in salsa emergenziale. Il potentino che voleva “vaccinare chiunque passa“, tuttavia, continua a conservare l’incarico istituzionale all’interno del Comando Operativo di Vertice Interforze, senza rossore alcuno per il ministero della Difesa. Passando a Draghi, secondo gli osservatori mainstream dopo l’uscita di scena di Berlusconi (che avevamo anticipato e che non abbiamo mai considerato come opzione), si prospetterebbe la corsa al Colle, ma anche qui potrebbe trattarsi del solito bluff per spianare la strada al vero candidato che metterebbe tutti d’accordo. Insomma, messa da parte la politica, a restare sul tavolo sono le migliaia di pagine presentate all’attenzione delle Procure di tutta Italia, che comunque potrebbero avere ovvie ripercussioni anche sulle scelte di partiti che non intendono rimanere imbrigliati in affari giudiziari.
Il generale accusato di omicidio colposo, crimini contro l’Umanità, abuso di autorità, violenza privata, procurato allarme e diffusione di notizie false
Per quanto riguarda Figliuolo, sono pesantissime le accuse formulate dall’ingegnere Giuseppe Reda, il ricercatore dell’Unical che ha denunciato l’operato del militare alla Procura della Repubblica di Reggio Emilia. Sotto la lente degli inquirenti finirà il papello di riferimenti alle misure controverse che secondo Reda ha reso colpevole Figliuolo dei reati di abuso di autorità, violenza privata, diffusione di notizie false atte a turbare l’ordine pubblico, procurato allarme, omicidio colposo, crimini contro l’umanità, violazione della Costituzione Italiana agli art. 2, 32, 54, 76, 78. Di più: Figliuolo ha ammesso candidamente di essere stato al servizio della sperimentazione umana in Italia dei preparati cosiddetti anti-covid: “Mai nella storia dell’uomo – sono le dichiarazioni gravi fatte dal militare in Piemonte alla presenza di Alberto Cirio – si è iniettato in pochissimo tempo decine di milioni di dosi di vaccini, senza saperne esattamente l’esito. Se non quello sperimentale che ha portato all’approvazione da parte della comunità scientifica”.
In fila per denunciare Draghi
A Biella, addirittura, pur di denunciare Mario Draghi e il suo operato ci si mette in fila. Nel mirino, la gestione della pandemia alla Conte, con un Dpcm dietro l’altro con il fine di introdurre una sorta di obbligo vaccinale di fatto e di estorcere la vaccinazione anche in chi – in realtà – non avrebbe voluto sottoporvisi. Una condotta che per i denuncianti avrebbe comportato la violazione dell’articolo 610 del codice penale, che recita che “chiunque, con violenza o minaccia, costringe altri a fare, tollerare od omettere qualche cosa è punito con la reclusione fino a quattro anni”. E non è vero, come riporta La Stampa, che si tratta di istanze senza futuro, perché “dal 20 non si potrà più agire in giudizio per la propria tutela personale, in quanto per potervi accedere bisognerà esibire l’infame tessera verde”: perfino il decreto del 7 gennaio – nei fatti – specifica che denuncianti, testimoni e accusati sono esentati dalla presentazione del Green Pass. A Messina, Draghi e il governo sono stati denunciati per sequestro di persona e violenza privata, per aver impedito ai siciliani – perfino a chi doveva spostarsi per necessità chirurgiche – di raggiungere la Penisola in forza dei blocchi imposti all’imbarco dei traghetti tramite l’introduzione del Green Pass. A Varese, ancora, pioggia di denunce per le discriminazioni compiute dall’esecutivo e dal premier ai danni di chi non si è voluto o potuto vaccinare, ma la lista sembra essere più lunga e alimentarsi di ora in ora.
La querela di ALI contro Draghi, Conte Speranza per i delitti commessi contro la personalità dello Stato, tra cui eversione dell’ordine democratico, cospirazione, attentato contro la Costituzione e gli organi costituzionali
C’è poi – per ultima ma non da ultima – l’azione promossa dal team di legali che si sono uniti sotto la sigla ALI – Avvocati Liberi – che ha querelato il presidente del Consiglio Mario Draghi, il suo predecessore Giuseppe Conte e il ministro della Salute Roberto Speranza per diversi e gravi delitti “contro la personalità dello Stato”. Gli avvocati hanno presentato una querela di oltre 30 pagine, in cui si fa riferimento al reato di associazione con finalità di eversione dell’ordine democratico (articolo 270 bis c.p.), cospirazione politica mediante accordo (Art. 304 c.p.), Attentato contro la Costituzione dello Stato (Art. 283 c.p.), Attentato e atti violenti contro gli organi costituzionali e contro le Assemblee Regionali (Art. 289 c.p.), Attentato per finalità terroristiche o di eversione (Art. 280 c.p.), pubblica estorsione.





















Non otterranno mai lo stop delle vaccinazioni.